1 Inleiding
Invasieve schimmelinfecties kunnen worden onderverdeeld in infecties door schimmels (filamenteuze schimmelinfecties) en infecties door gisten. Aspergillus species en Candida species zijn verantwoordelijk voor het grootste deel van de invasieve schimmelinfecties1.
Andere belangrijke pathogenen zijn Mucorales species, Fusarium species en Scedosporium species, maar er zijn nog vele filamenteuze schimmels die sporadisch invasieve infecties veroorzaken. De diagnose van schimmelinfecties berust op patiëntkenmerken in combinatie met beeldvorming en mycologische testen, zoals kweek, directe microscopie, histopathologie, moleculaire testen, antigeenbepalingen en serologie2–5. De prestatie van de mycologische testen is sterk afhankelijk van de patiëntpopulatie en gebruik van antifungale profylaxe/behandeling6–8
2 Klinische beelden
Infecties met Aspergillus en verwante schimmels kunnen zich op verschillende manieren uiten. Deze ziektebeelden worden ingedeeld in functie van de snelheid waarmee ze zich ontwikkelen (acuut – subacuut – chronisch), het aangetaste orgaan, en de reactie van het immuunsysteem hierop9.
Aangezien Aspergillus sporen alomtegenwoordig zijn in de lucht en continu worden ingeademd, zijn de luchtwegen en sinussen de meest frequente plaats waar ziekte ontstaat10. Er kan echter ook extrapulmonale aantasting in elk ander orgaan ontstaan na initiële infectie in de longen, of er kan een primaire infectie ontstaan in elk ander orgaan, zeker als er een extern trauma is met contaminatie met sporen9. Aantasting in andere organen is vaak moeilijk vast te stellen aangezien dit een zeldzame lokalisatie is, en er dus vaak pas laat aan gedacht wordt, wat de prognose ongunstig beïnvloedt11,12.
In figuur 1 staan de belangrijkste ziektebeelden die door Aspergillus veroorzaakt worden schematisch afgebeeld, in functie van de respons van het immuunsysteem.
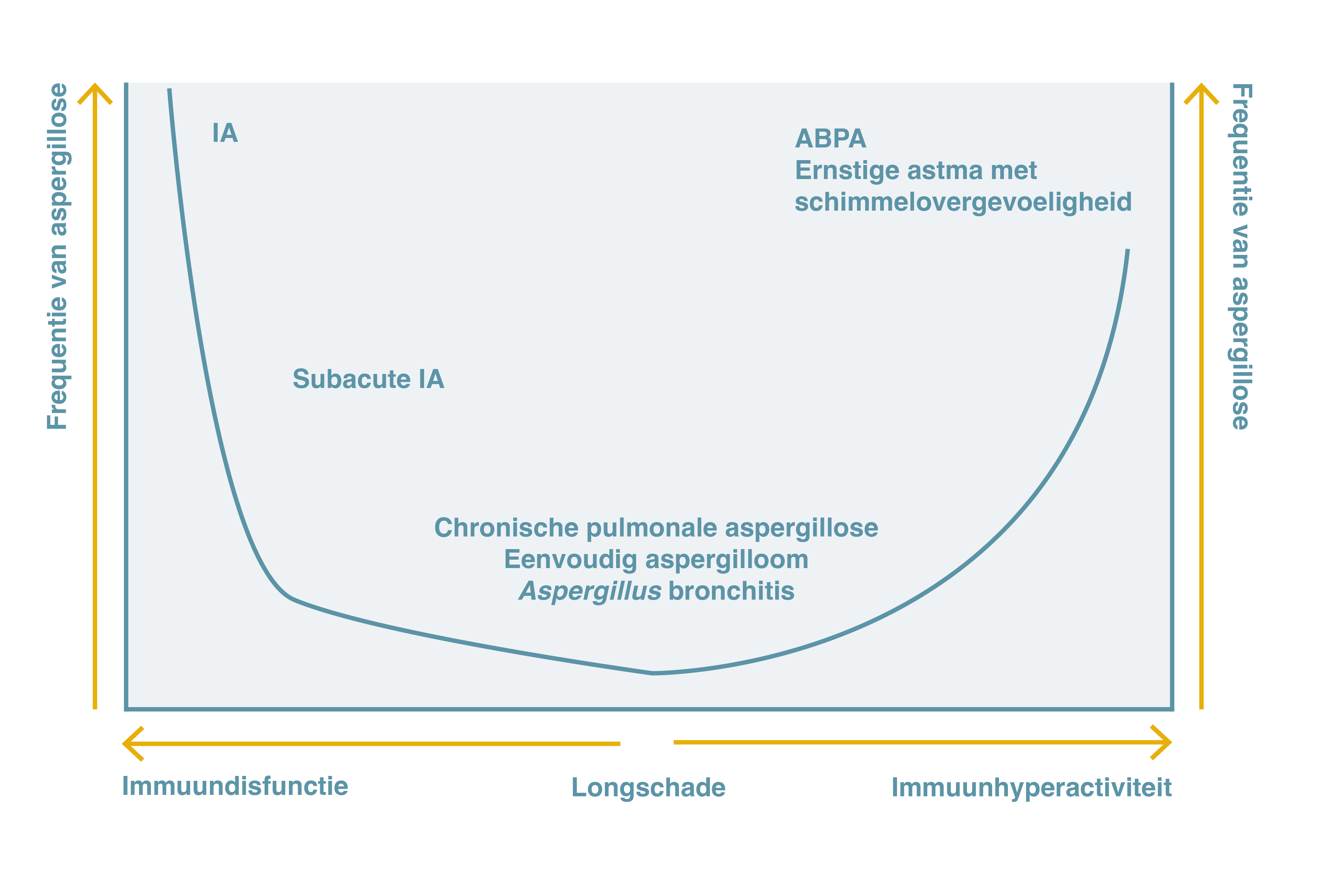
Figuur 1. Het klinische spectrum van Pulmonale Aspergillose Overgenomen en bewerkt van Kosmidis C et al. 20159
ABPA=Allergische bronchopulmonale aspergillose
Allergische beelden
Bij patiënten met mucoviscidose/cystic fibrosis, ernstig astma, en aanverwante respiratoire aandoeningen, kan een IgE-gemedieerde allergie aan Aspergillus de oorzaak en onderhoudende factor zijn voor uitgesproken respiratoire klachten die moeilijk onder controle te brengen zijn13–17. Meest frequent gaat het dan om dyspnoe, constitutionele symptomen, hemoptoë en hoest. Aangezien de klachten veroorzaakt worden door een overreactie op de schimmel, bestaat de behandeling meestal uit het onderdrukken van zowel de schimmel als de respons hierop, door middel van immunosuppressiva (zoals corticosteroïden), al dan niet in combinatie met antifungale middelen15.
Chronische pulmonale aspergillose (CPA)
Wanneer er structurele defecten in de luchtwegen zijn, zoals bijvoorbeeld holtevorming na een doorgemaakte pulmonale tuberculosis, maar echter ook in normale sinusholtes, dan kan Aspergillus hier een ideaal milieu vinden om in te groeien18. Bij patiënten met een voldoende intact immuunsysteem zal de groei beperkt worden tot aan de randen van deze holte d.m.v. een afweerreactie van het aangeboren immuunsysteem, via onder andere T-cel immuniteit en circulerende patroonherkenningsreceptoren zoals pentraxine-319. Door de holtevorming kan het immuunsysteem echter niet voldoende doordringen waardoor er een chronische infectie met de bijbehorende symptomen hoort, zoals koorts, nachtzweten, malaise en vermagering, evenals lokale symptomen zoals dyspnoe, hoest of hemoptoë18.
Op CT kan de schimmelbal zichtbaar zijn in een holte: dit wordt een aspergilloom genoemd. Verder kunnen ook kleinere nodules, infiltraten, en fibrose zichtbaar zijn in variabele mate20.
Invasieve aspergillose (IA)
Wanneer het immuunsysteem zodanig onderdrukt is dat de schimmel vrij doorheen de normale barrières kan groeien, spreken we van een invasieve fungale infectie. In de longen kan dit zowel “airway invasive” zijn wanneer het doorheen de bronchi groeit, als “angio-invasive” wanneer ook de bloedvaten doorbroken worden. Dit ontstaat typisch enkel bij zeer sterk immuungecompromiteerde patiënten zoals bij hematologische ziektes, hoge dosis corticosteroïden, kritisch zieke patiënten, of aangeboren immuundeficiënties21. Meer uitgebreide risicogroepen vindt u in hoofdstuk 3.
De symptomen en afwijkingen zijn afhankelijk van de lokalisatie10. Zo zal bij een invasieve infectie er meestal koorts en/of een verhoogd CRP zijn, in combinatie met focale klachten. Een pulmonale infectie (invasieve pulmonale aspergillose, IPA) veroorzaakt bijvoorbeeld soms hemoptoë of pleurale pijn, maar dit kan evengoed zonder lokaliserende klachten verlopen. Sinusitis geeft dan weer zeer uitgesproken gelaatspijnen. Wanneer de schimmel door de botstructuren heen groeit, kunnen ook de faciale zenuwen uitvallen en kan er exoftalmie ontstaan door druk op de oogbol. Bij aantasting van het centrale zenuwstelsel kan er focale uitval zijn of algemene achteruitgang, en bij aantasting van de huid en weke delen ontstaat er een uitbreidende verkleuring, vaak met ischemische pijnen.
Aangezien elk orgaan aangetast kan worden, is het spectrum aan mogelijke klachten en afwijkingen bij IA in principe onbeperkt. Het belangrijkste bij IA is dan ook om steeds aan een fungale infectie te denken bij een risicopatiënt met onverklaarde klachten, en snel en gericht onderzoek hiernaar te doen22.
In de hierop volgende hoofdstukken focussen we ons verder voornamelijk op invasieve aspergillose.
3 Risicogroepen
De meeste invasieve schimmelinfecties zijn opportunistische infecties. Patiënten die vatbaar zijn voor invasieve schimmelinfecties zijn ernstig immuungecompromitteerde patiënten.
Invasieve schimmelinfecties komen voornamelijk voor bij patiënten met langdurige neutropenie, patiënten die een stamceltransplantatie ondergaan, patiënten die langdurig hoge dosis corticosteroïden gebruiken, patiënten die een longtransplantatie ondergaan en patiënten met primaire immuunstoornissen zoals chronische granulomateuze ziekte (CGD)21. Bij patiënten met andere orgaantransplantaties komen invasieve schimmelinfecties ook voor, doch in mindere mate21. Naast patiënten met een immuunstoornis kunnen ook kritisch zieke patiënten die zijn opgenomen op de intensive care unit een invasieve schimmelinfectie ontwikkelen, voornamelijk kritisch zieke patiënten met een influenza of Covid-19 infectie23–25.
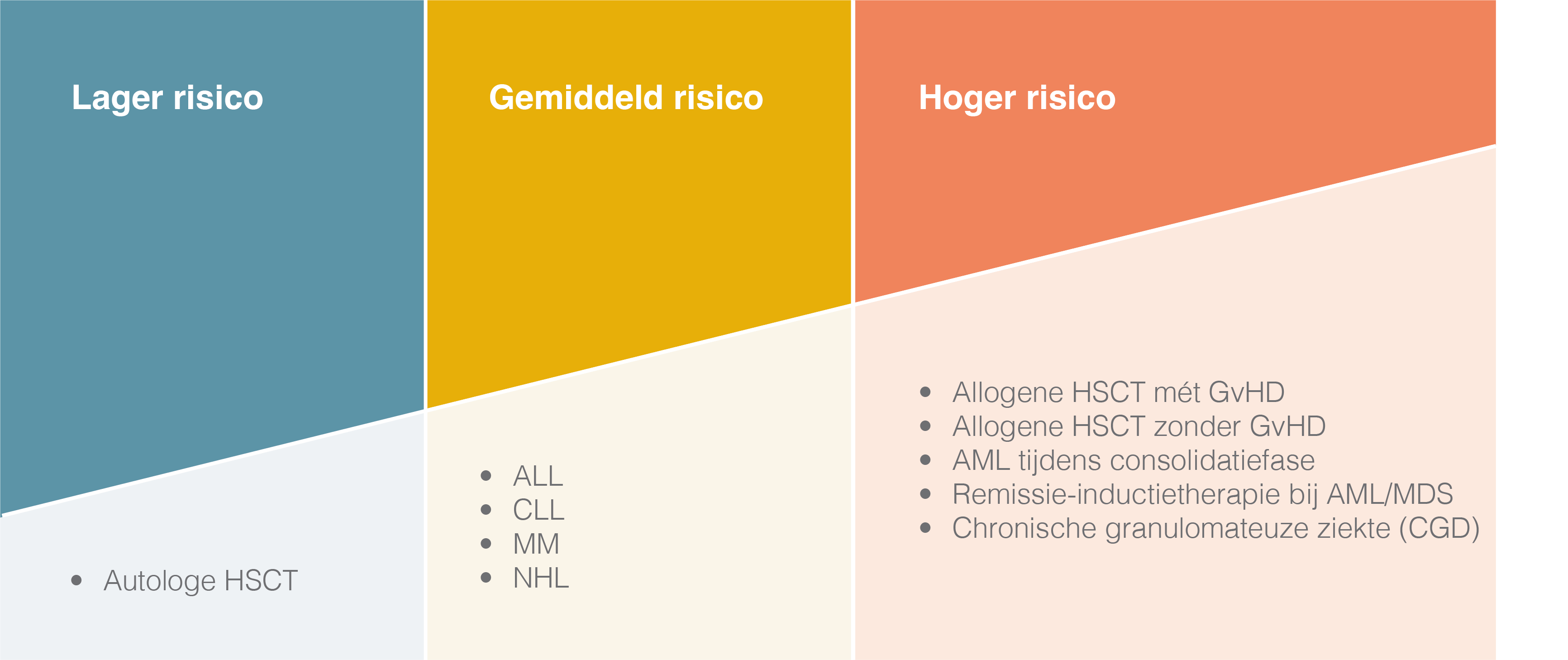
Figuur 2. Het risico op invasieve aspergillose door hematologisch ziektebeeld of behandeling. Overgenomen en bewerkt van Herbrecht R et al. 201272
4 Diagnostiek + pitfalls
De diagnostiek van IA is bij voorkeur gebaseerd op drie pijlers:
- Een vatbare patiënt met compatibele klinische afwijkingen of klachten
- Suggestieve objectieve afwijkingen op beeldvorming of invasieve onderzoeken
- Aantonen van de aanwezigheid van Aspergillus of een andere schimmel
De combinatie van deze drie pijlers geeft de hoogste waarschijnlijkheid op de aanwezigheid van een invasieve fungale infectie2,3,5,26. Echter, de enige manier om dit met zekerheid aan te tonen is door het nemen van een biopsie met aantonen van invasieve groei, of alternatief, het kweken van de schimmel uit een steriele ruimte26. Dit is in de praktijk echter vaak niet haalbaar. Er moet dan ook bij elke patiënt gestreefd worden naar een zo compleet mogelijke diagnostiek om onder- en overbehandeling te vermijden22.
Medische beeldvorming
Als er bij een vatbare patiënt een verdenking is op IA op basis van het klinisch beeld, bestaat de eerste stap uit het in beeld brengen van de verdachte lokalisatie(s) aangezien de meeste infecties zich diep in het lichaam bevinden3,5. Enkel bij geïsoleerde cutane infectie is beeldvorming niet strikt genomen aangewezen, hoewel er in sommige expertisecentra wel routinematig beeldvorming gebeurt van de longen en de hersenen als er elders een fungale infectie vastgesteld werd.
Het onderzoek voor pulmonale IA dat de voorkeur heeft is een hoge resolutie CT-thorax3,5. Bij neutropene patiënten kunnen hier de klassieke beelden gezien worden van dense, welomschreven nodules, al dan niet met omliggend matglas (het zogeheten “halo sign”, wat wijst op angio-invasie en invasie door reactieve leukocyten), “air-crescent sign” waarbij een luchtsikkel zichtbaar is rondom een fungale bal (compatibel met laattijdige infectie), en meer uitgebreide consolidaties27. Deze tekens zijn echter niet uniek voor IA, en kunnen evengoed gezien worden bij andere fungale of bacteriële infecties, evenals bij auto-immune of maligne processen28.
Om te helpen onderscheiden tussen invasieve schimmelinfecties en andere oorzaken van nodules, kan het nuttig zijn een pulmonale angiografie te doen (CTPA), gelijkaardig aan het protocol gebruikt bij longembolieën. Uit Duits onderzoek bleek de aanwezigheid van een nodule die de bloedvaten onderbreekt (“vessel occlusion sign”) een sensitief en specifiek teken voor angio-invasieve IA, dat onderscheid mogelijk maakt met andere infectieuze, maligne en inflammatoire processen waarbij de bloedvaten net wel doorheen de nodule gaan29,30.
In de opvolging van het effect van antifungale therapie is het belangrijk de CT niet te snel te herhalen. Zeker als er immuunreconstitutie is (bijvoorbeeld door herstel van neutropenie of afbouw van corticosteroïden) kunnen de letsels gedurende de eerste twee weken nog toenemen door influx van leukocyten31. Nadien is CT wel een belangrijk middel om de evolutie van de infectie op te volgen, en zal dit mee de termijn van behandeling bepalen32.
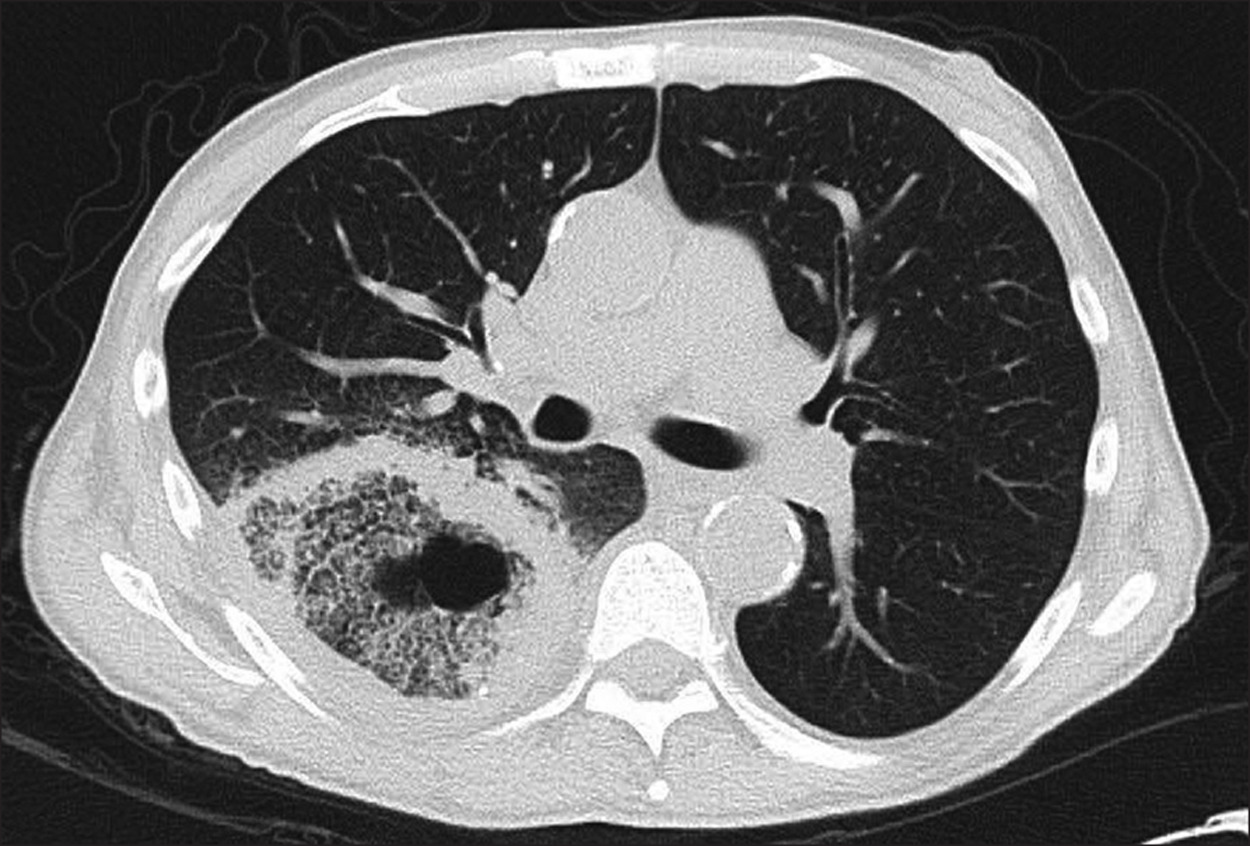
Omgekeerd haloteken bij mucormycosis
Overgenomen uit: Wang et al. Clinical diagnostic value of spiral CT in invasive pulmonary fungal infection. Exp Ther Med. 2019;17(5):4149-4153.
Bij aantasting van het centraal zenuwstelsel kan een CT gebeuren, waarbij parenchymale abcesvorming of lokale versterkte tekening van de hersenvliezen gezien kan worden26. Specifieke MRI-sequenties werden ontwikkeld die verder helpen het onderscheid te maken in de origine van cerebrale letsels33–35.
Bij vermoeden van invasieve sinusitis is CT (spiraal of cone beam) het voorkeursonderzoek3,5. Bij invasieve ziekte wordt er naast mucosale defecten ook in de regel botdoorbraak gezien26. Bij beginnende ziekte kan dit soms niet meteen goed zichtbaar zijn. Bij persisterende uitgesproken, onverklaarde sinusale pijn kan het daarom eventueel de moeite lonen om het onderzoek te herhalen
Tot slot is ook FDG-PET-CT een nuttig onderzoek als er een vermoeden van een fungale infectie is, zonder dat er lokaliserende klinische klachten zijn, en indien de meest typische lokalisaties (longen) normaal blijken36. Ook hier geldt uiteraard dat PET-CT geen verdere details geeft over de letsels: FDG-avide letsels kunnen evengoed passen bij maligniteiten, andere infecties of auto-immuniteit. Het laat wel toe om gerichte biopsie te doen om zo de verdere aard van het proces te bepalen. Ook bij patiënten bij wie er al indirecte tekens van IA zijn, zoals een verhoogd serum galactomannan en onverklaarde koorts, kan een PET-CT op zich voldoende zijn om een vermoedelijke diagnose van IA te stellen en behandeling op te starten indien lokale biopt niet mogelijk is.
Invasieve onderzoeken (broncho, FEES,..)
Op het moment dat er door middel van beeldvorming en suggestieve kliniek een sterk vermoeden is van IA, is gerichte biopsie aangeraden5,22. Bij pulmonale aantasting kan dit d.m.v. bronchoscopie met afname van bronchoalveolair lavage vocht (BAL), bij sinustis via flexibele endoscopie, bij CNS-lokalisatie d.m.v. een lumbaalpunctie, enzoverder. Zo mogelijk kan er ook een biopsie genomen worden, maar uiteraard dienen de risico’s hiervan goed afgewogen te worden t.o.v. de voordelen.
Naast biopt laten deze onderzoeken ook de visu inspectie van de inwendige organen toe. Zo kunnen er bij Aspergillus sinusitis of tracheobronchitis intern witte plaques, nodules, pseudemembranen, ulcera en bloedingen gezien worden10,26.
Indirecte testen
Bij indirecte testen wordt er gepoogd om de aanwezigheid van een schimmel indirect aan te tonen d.m.v. detectie van bepaalde celwandcomponenten of fungaal DNA. Deze testen zijn in de regel gevoeliger dan de klassieke kweek: ongeveer ¼ van de kweken is negatief, versus een sensitiviteit tussen de 80 – 100% voor de meeste indirecte testen22. Het nadeel is uiteraard dat er met de meeste indirecte testen geen gevoeligheidsbepaling mogelijk is, noch exacte identificatie van het pathogeen, of detectie van co-infectie. Deze testen vervangen de klassieke kweek dus niet!
GM ELISA
Galactomannan (GM) is een celwandcomponent van Aspergillus en enkele aanverwante schimmels (o.a. Fusarium, Histoplasma, Penicillium/Talaromyces)37–40. Dit kan gedetecteerd worden d.m.v. een sandwich ELISA (Platelia assay, Bio-Rad). Deze test is FDA labeled en CE-marked voor detectie van galactomannan in serum en BAL, maar wordt eveneens gebruikt in cerebrospinaal vocht en andere typen lichaamsvocht met verdenking op invasieve aspergillose41. De cutoff-waarde voor positiviteit varieert afhankelijk van de geteste matrix: op bloed wordt er geen contaminatie of kolonisatie verwacht, en is de cutoff 0.5 ODI. De luchtwegen bevatten vaker een kleine hoeveelheid Aspergillus als kolonisatie, waardoor een hogere cutoff van 1.0 ODI de specificiteit verhoogt zonder de gevoeligheid van de test te veel te verlagen. De sensitiviteit van de test is merkbaar lager bij niet-neutropene patiënten wanneer toegepast op serum (niet op BAL), en bij mensen onder mould-active profylaxe6,42,43.
Aangezien Aspergillus vaak ook in industriële processen wordt gebruikt voor het maken van organische moleculen, kan hierbij GM terecht komen in het eindproduct44. Toediening hiervan kan zo resulteren in vals verhoogde GM-waardes in het bloed. Typische voorbeelden hiervan zijn de beta-lactamantibiotica of gebalanceerde elektrolytoplossingen, hoewel fabrikanten in de afgelopen jaren stappen hebben ondernomen om GM uit hun producten te elimineren45.
Lateral flow
Sinds enkele jaren zijn er lateral flow testen voor Aspergillus op de markt. Deze worden ook wel verkocht als “sneltest” of als “point of care test”, naar analogie met bijvoorbeeld de SARS-CoV-2 sneltesten die men thuis kan uitvoeren. Deze vergelijking gaat echter niet op voor de testen die momenteel commercieel beschikbaar zijn (OLM AspLFD & IMMY Sōna Aspergillus GM Lateral Flow Assay) aangezien beiden steeds het gebruik van micropipetten, en meestal ook centrifuges en verhittingsblokken vereisen46. Ze zijn echter wel optimaal voor centra waar de turnaround tijd voor klassieke galactomannan testing te lang oploopt omwille van batching, of omdat de test extern verzonden moet worden. In deze gevallen kan een lateral flow test eenvoudig en snel in het eigen microbiologisch lab gebeuren. De diagnostische accuraatheid is gelijkaardig (IMMY) of licht inferieur (OLM) aan deze van de Platelia® galactomannan assay, doch voor beiden voldoende voor de routine diagnostiek47,48.
BDG
Beta-D-glucan (BDG) is een structureel onderdeel van de celwand van zo goed als alle fungi. Het is dan ook een ideale biomarker voor de aanwezigheid van schimmels49,50. Het nadeel van deze “pan-fungale” biomarker is uiteraard dat het geen verdere details geeft over welke fungale infectie er actief is. De hoeveelheid BDG in het bloed is wel indicatief voor het type infectie: bij Pneumocystis worden er typisch zeer hoge waarden gezien, terwijl dit bij andere infecties eerder randverhoogd is51–53. Uiteraard zijn uitzonderingen op beide situaties altijd mogelijk. Er zijn verschillende assays op de markt, elk met eigen referentiewaarden; de waarden van 2 verschillende assays zijn onderling niet vergelijkbaar54. De assays hebben wel een gelijkaardig diagnostische accuraatheid en verschillen vooral in hun praktische aspecten54,55.
Net zoals bij GM, kan ook BDG vals verhoogd zijn door toediening van organische componenten waarbij schimmels gebruikt werden in de productie, of die BDG bevatten om andere redenen. De meest frequente bronnen hiervan zijn IV-immuunglobulines, IV-albumine, cellulose kompressen, cellulose filters (bijvoorbeeld bij hemodialyse) en beta-lactam antibiotica56.
PCR inclusief resistentie
Moleculaire methoden, zoals PCR, worden gebruikt voor de snelle en specifieke detectie van schimmels. Er zijn verschillende soorten PCR tests beschikbaar, waaronder rt-PCR tests die specifiek Aspergillus species kunnen aantonen en tests die specifiek Aspergillus fumigatus kunnen detecteren en tegelijkertijd markers voor azoolresistentie kunnen aantonen57. De gevoeligheid van een PCR op een BAL voor het aantonen van Aspergillus is hoog, maar het kan geen goed onderscheid maken tussen kolonisatie en een daadwerkelijke infectie58. PCR kan ook worden gebruikt op een weefselsample afgenomen door middel van biopsie of op liquor bij een vermoeden van een cerebrale aspergillose59,60. Er wordt ook veel onderzoek gedaan naar de meerwaarde van PCR op serumsamples61. Aangezien de detectie van Aspergillus gebaseerd is op een multicopy gen, terwijl het aantonen van azoolresistentie op basis van een singlycopy gen is, is de gevoeligheid van het aantonen van azoolresistentie lager en kan slechts in 50-70% van de gevallen met een positieve Aspergillus-PCR de resistentie worden uitgesloten57.
De huidige beschikbare methoden zijn gericht op het aantonen van TR34/L98H en TR46/Y121F/T289A. Deze twee resistentiemechanismen zijn verantwoordelijk voor 90% van de azoolresistentie bij A. fumigatus62. Als er een Aspergillus is gekweekt, moet dit altijd worden gecombineerd met fenotypische gevoeligheid omdat enkele resistentie mechanismen niet worden aangetoond met de moleculaire methoden63.
Er zijn ook moleculaire methoden ontwikkeld voor Mucorales species, waaronder PCR op serum, die een goede gevoeligheid heeft bij patiënten met een invasieve mucormycose64,65.
Directe testen
Kweken
De meeste schimmels kunnen worden gedetecteerd door middel van kweek, maar de gevoeligheid hiervan is beperkt en het kan enkele dagen tot weken duren voordat een kweek positief is3,5,66. Geschikte monsters voor kweek zijn onder andere sputum en BAL, maar ook weefselmonsters. Als uit een gewoonlijk steriel weefselmonster een schimmel wordt gekweekt, is dit bewijs voor een schimmelinfectie26.
Bij een positieve kweek van een respiratoir materiaal is dit niet het geval. Er kan dan op basis van kweek geen onderscheid worden gemaakt tussen kolonisatie en een daadwerkelijke infectie en moeten andere klinische en radiologische factoren worden meegenomen bij de interpretatie. Aangezien Aspergillus fumigatus in Nederland in 5-10% van de gevallen resistent is voor azolen, is het van belang om azoolresistentie uit te sluiten wanneer er een behandelindicatie is67. Gevoeligheidsbepaling van schimmels, waaronder Aspergillus fumigatus, is mogelijk, maar wordt slechts in enkele centra uitgevoerd. Er is een snelle screeningsmethode ontwikkeld voor azoolresistentie die makkelijk te implementeren is in lokale laboratoria, maar deze methode is alleen geschikt voor het uitsluiten van resistentie bij Aspergillus fumigatus en niet geschikt voor andere Aspergillus species68. Er is geen snelle screeningmethode beschikbaar voor andere schimmelsoorten.
Directe microscopie en histopathologie
Directe microscopie is een effectieve techniek voor het snel detecteren van schimmels in patiëntmateriaal, waaronder weefsel- en respiratoir materiaal22,69. Door gebruik te maken van fluorescerende kleurstoffen, zoals Blankophor en Calcofluor White, worden de schimmelcelwanden verlicht waardoor ze beter zichtbaar zijn onder een fluorescerende microscoop. Hierdoor kunnen schimmelstructuren snel en eenvoudig worden aangetoond.
Daarnaast kunnen schimmelstructuren worden aangetoond met behulp van histopathologische kleuringen22,69. BAL en weefsels verkregen met biopsie zijn hiervoor de meest geschikte materialen. De standaard H&E (hematoxyline en eosine) kleuring wordt gebruikt om te bepalen of er sprake is van ontsteking, maar is niet specifiek voor schimmels. Desondanks kunnen hyfen en schimmels met deze kleuring wel worden opgemerkt. Bij vermoedens van een schimmelinfectie kan het nuttig zijn om aanvullend een PAS (Periodic Acid-Schiff) en een Grocott’s (Grocott-Gomori’s methenamine silver) kleuring uit te voeren. Hiermee worden schimmeldraden specifiek aangekleurd, waardoor deze beter zichtbaar zijn en gebruikt kunnen worden om schimmeldraden in weefsel te detecteren.
Een nadeel van microscopie is de beperkte gevoeligheid22,69. Met behulp van microscopie kunnen schimmeldraden worden aangetoond, maar betrouwbare identificatie van de schimmel is niet mogelijk. Als er gesegmenteerde schimmeldraden worden gezien met dichotome vertakkingen zou dit bij een Aspergillus infectie kunnen passen. Echter ook veel andere schimmels kunnen dezelfde kenmerken hebben. Bij infecties door Mucorales worden juist geen of weinig segmenten gezien in de schimmeldraden, zijn de draden erg wisselend van diameter en vertakken de schimmeldraden recht (op 90 graden) af.
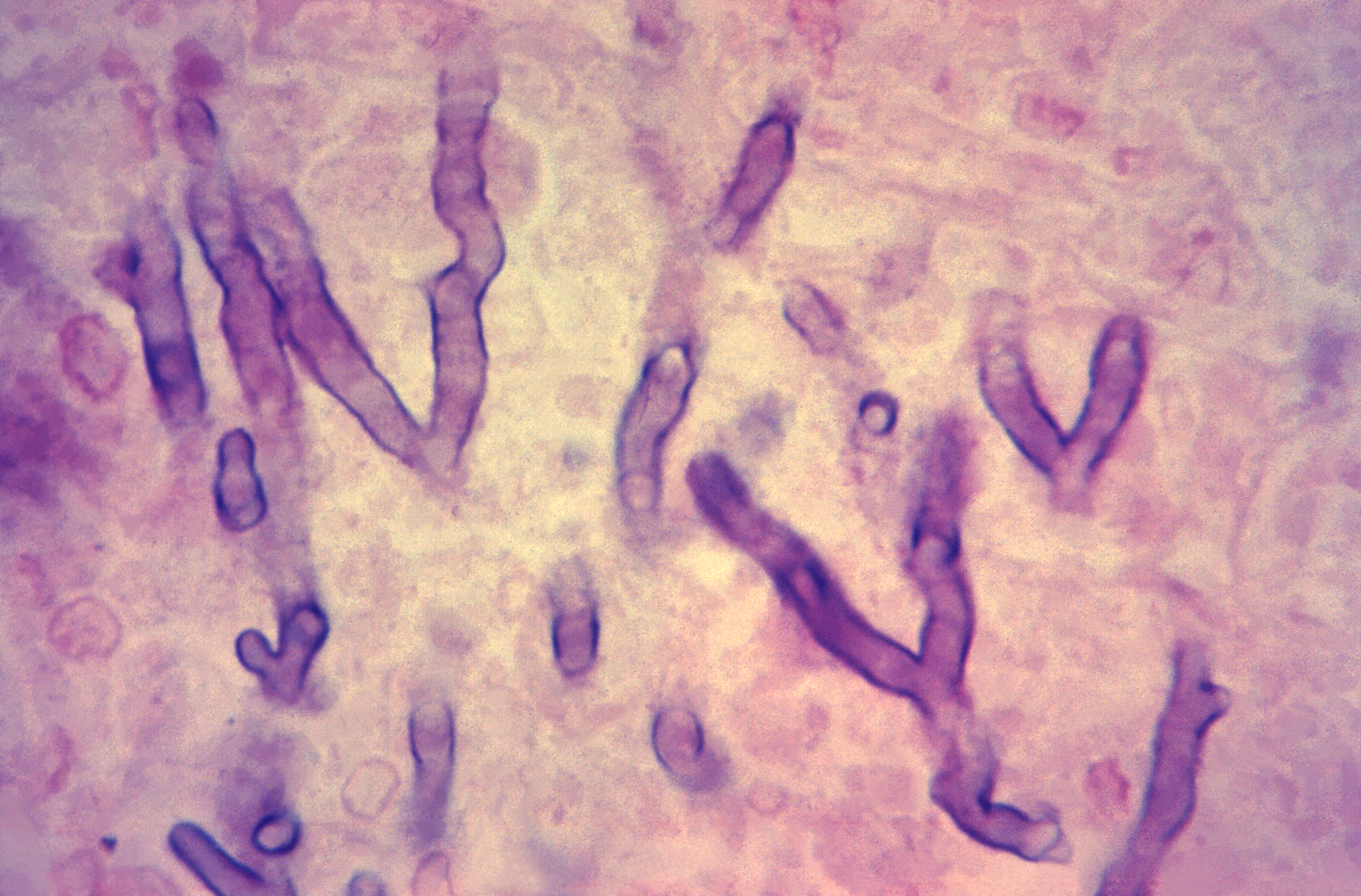
Deze microscopiefoto van een met hematoxyline-eosine (H&E) gekleurd menselijk longweefselmonster, geoogst van een patiënt met pulmonale aspergillose, toont de histopathologische veranderingen door de aanwezigheid van Aspergillus sp. schimmelorganismen. Let op de vertakkende hyfen tussen het longweefsel.
Bron: CDC/ Armed Forces Institute of Pathology (AFIP); Dr. Hardin:
https://phil.cdc.gov/Details.aspx?pid=15630
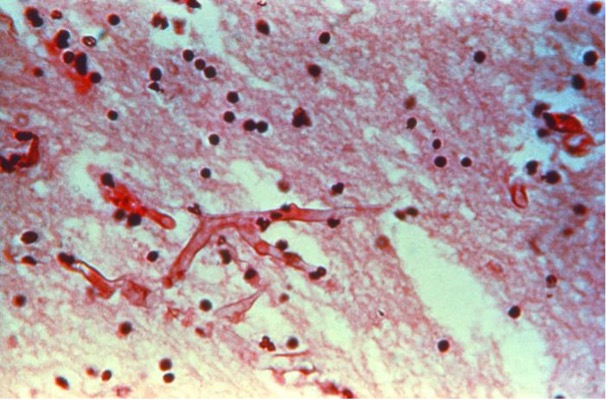
Microscopiefoto van (hematoxyline-eosine (HE)-gekleurd menselijk longweefsel toont de aanwezigheid van myceliumschimmelfilamenten bij een patiënt met mucormycose (phycomycose), ook wel bekend als een vorm van zygomycose.
Bron: CDC/ Dr. Lucille K. Georg
5 Toepassing op klinische situaties
Casus 1: AML-patiënt met pijnlijk leasies
64-jarige patiënt met AML waarvoor remissie inductietherapie. Op dag 10 van neutropenie ontwikkelt patiënt koorts waarvoor ceftazidim is gestart. Na 3 dagen heeft patiënt echter nog steeds koorts. De bloedkweken zijn nog negatief.
CT-scan van long en sinussen toont geen aanwijzing voor een schimmelinfectie. Serum galactomannan van dag 10 is 1.2 (Bio-Rad) en op dag 11 is de Galactomannan 1.5. In de loop van de dagen ontwikkeld patiënt enkele pijnlijke laesies met centrale necrose op zijn arm.
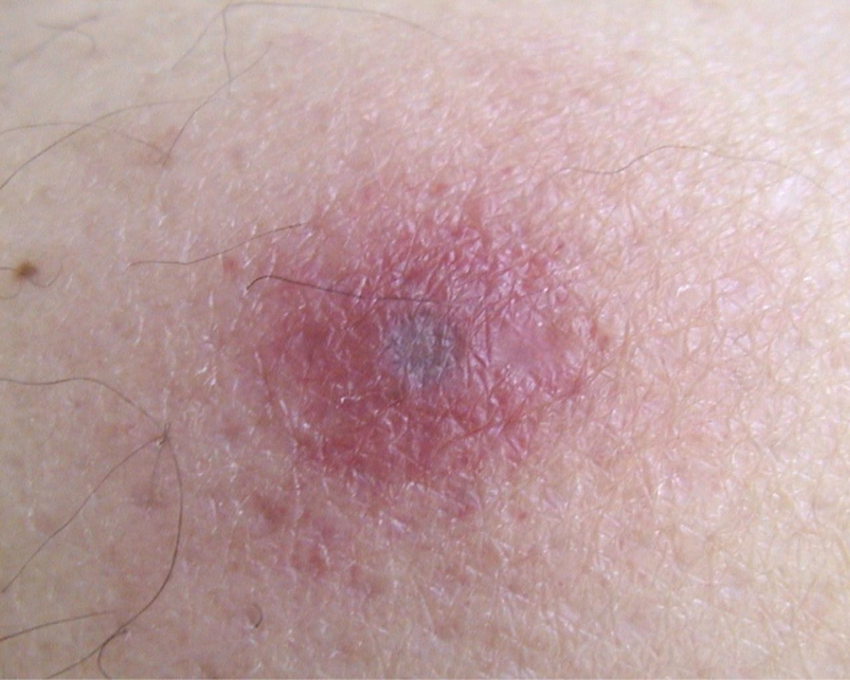
Gedissemineerde invasieve fusariose (Researchgate)
Bron: Researchgate: Juan Ambrosioni
Casus 2: AML-patiënt met aanhoudende koorts op schimmel profylaxe
Een 48-jarige vrouw wordt opgenomen met nieuwe diagnose van AML en start met klassieke inductiechemotherapie, onder dekking van o.a. posaconazole profylaxe. Na 10 dagen ontstaat er neutropene koorts waarvoor Cefepime wordt opgestart. Bloedkweken blijven negatief. Ondanks 5 dagen breedspectrum antibiotica, blijft de patiënt koorts maken. Bij uitgebreid klinisch onderzoek zijn er geen richtinggevende klachten of symptomen.
Casus 3: IAPA
Een patiënt meldt zich op de Spoedeisende Hulp (SEH) met een respiratoire insufficiëntie. Voorgeschiedenis vermeldt een COPD waarvoor de patiënt recent corticosteroïden had voorgeschreven gekregen, een recente galweg operatie, en een depressie waarvoor patiënt lithium gebruikt. Er wordt een PCR-influenza afgenomen op een nasopharynx spoeling die positief blijkt. In verband met respiratoire achteruitgang wordt de patiënt al snel overgeplaatst naar de IC voor invasieve beademing.
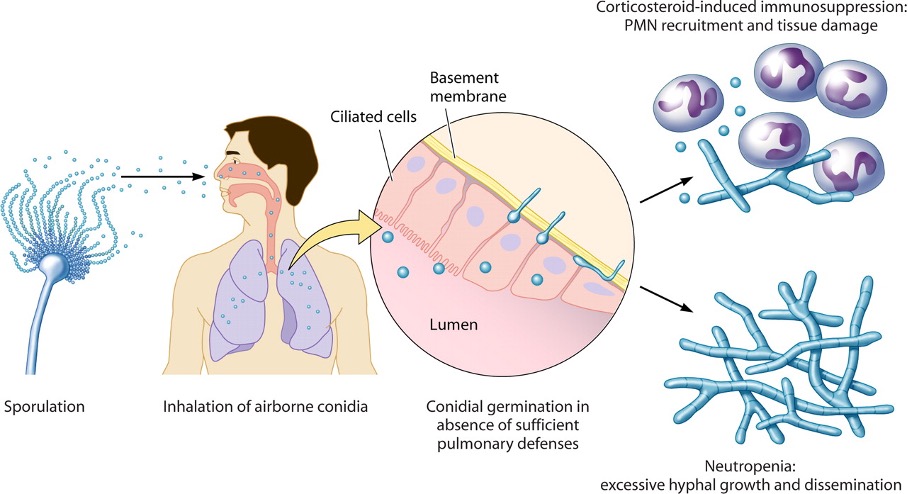
Infectieuze levenscyclus van A. fumigatus. Aspergillus is alomtegenwoordig in het milieu en ongeslachtelijke voortplanting leidt tot de productie van conidia in de lucht. Inhalatie door specifieke groepen patiënten met immunosuppressie resulteert in de vestiging van conidium in de longen, kieming en PMN-gemedieerde schimmelcontrole met significante ontsteking (therapie met corticosteroïden) of ongecontroleerde hyfengroei met een gebrek aan PMN-infiltraten en, in ernstige gevallen, verspreiding (neutropenie).
Bron: T. Dagenais et al, 2009
Referenties patiëntencasussen
Algemeen
Kosmidis & Denning, Thorax. 2015 Mar;70(3):270-7. doi: 10.1136/thoraxjnl-2014-206291.
Donnelly et al, Clin Infect Dis. 2020 Sep 12;71(6):1367-1376. doi: 10.1093/cid/ciz1008.
Richtlijnen
Richtlijn aspergillose 2017 ESCMID-ECMM-ERS guideline: Clin Microbiol Infect. 2018 May;24 Suppl 1:e1-e38.
Richtlijn aspergillose 2016 IDSA: Clin Infect Dis. 2016 Aug 15;63(4):e1-e60
Richtlijn schimmelinfecties Nederland, oa aspergillose en mucormycose: SWAB invasive mould infections
Specifieke onderwerpen
Serologie: Clin Microbiol Infect. 2021 Sep;27(9):1230-1241
IAPA: Intensive Care Medicine. 2020 46, 1524–1535
Colofon
Deze diagnosehulp is ontwikkeld door Jochem Buil en Toine Mercier.
“Schimmelinfecties zijn zeer variabel in hun presentatie en vragen een gerichte aanpak bij de diagnose en behandeling. Aangezien deze infecties eerder zeldzaam zijn, is het voor veel clinici moeilijk om hier veel praktische ervaring mee op te bouwen. Daarom ontwikkelden we deze beknopte diagnostische tool om als houvast te gebruiken. De belangrijkste pijlers van de diagnose staan overzichtelijk op de eerste pagina, en linken meteen door naar de juiste pagina waar meer uitgebreide achtergrondinformatie is te vinden”

Jochem Buil
is werkzaam als klinisch microbioloog in het RadboudUMC. Op de hoogte blijven van activiteiten van Jochem? Contactgegevens: jochem.buil@radboudumc.nl

Toine Mercier
is staflid hematologie in het AZ Sint-Maarten (Mechelen), consulent in het UZ Leuven, en onderzoeker aan de KU Leuven in België. Contactgegevens: toine.mercier@kuleuven.be
Referenties
1. Michael A. Pfaller, Peter G. Pappas, John R. Wingard Invasive Fungal Pathogens: Current Epidemiological Trends, Clinical Infectious Diseases 2006; 43, Suppl 1, S3–S14
2. Cornely OA, Arikan-Akdagli S, Dannaoui E, et al. ESCMID and ECMM joint clinical guidelines for the diagnosis and management of mucormycosis 2013. Clin Microbiol Infect 2014;20 Suppl 3:5–26.
3. Ullmann AJ, Aguado JM, Arikan-Akdagli S, et al. Diagnosis and management of Aspergillus diseases: executive summary of the 2017 ESCMID-ECMM-ERS guideline. Clinical Microbiology and Infection 2018;24:e1–38.
4. Tissot F, Agrawal S, Pagano L, et al. ECIL-6 guidelines for the treatment of invasive candidiasis, aspergillosis and mucormycosis in leukemia and hematopoietic stem cell transplant patients. Haematologica 2017;102(3):433–44.
5. Patterson TF, Thompson GR, Denning DW, et al. Practice Guidelines for the Diagnosis and Management of Aspergillosis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis 2016;63(4):e1–60.
6. Pfeiffer CD, Fine JP, Safdar N. Diagnosis of Invasive Aspergillosis Using a Galactomannan Assay: A Meta-Analysis. Clin Infect Dis 2006;42(10):1417–727.
7. Eigl S, Prattes J, Reinwald M, et al. Influence of mould-active antifungal treatment on the performance of the Aspergillus-specific bronchoalveolar lavage fluid lateral-flow device test. Int J Antimicrob Agents 2015;46(4):401–5.
8. Aguado JM, Vázquez L, Fernández-Ruiz M, et al. Serum galactomannan versus a combination of galactomannan and polymerase chain reaction-based Aspergillus DNA detection for early therapy of invasive aspergillosis in high-risk hematological patients: a randomized controlled trial. Clin Infect Dis 2015;60(3):405–14.
9. Kosmidis C, Denning DW. The clinical spectrum of pulmonary aspergillosis. Thorax 2015;70(3):270–7.
10. Muñoz P, Guinea J, Bouza E. Update on invasive aspergillosis: clinical and diagnostic aspects. Clinical Microbiology and Infection 2006;12(s7):24–39.
11. von Eiff M, Roos N, Schulten R, Hesse M, Zühlsdorf M, van de Loo J. Pulmonary aspergillosis: early diagnosis improves survival. Respiration 1995;62(6):341–7.
12. Chamilos G, Lewis RE, Kontoyiannis DP. Delaying Amphotericin B–Based Frontline Therapy Significantly Increases Mortality among Patients with Hematologic Malignancy Who Have Zygomycosis. Clin Infect Dis 2008;47(4):503–9.
13. Tracy MC, Okorie CUA, Foley EA, Moss RB. Allergic Bronchopulmonary Aspergillosis. Journal of Fungi 2016;2(2):17.
14. Hogaboam CM, Carpenter KJ, Schuh JM, Buckland KF. Aspergillus and asthma — any link? Medical Mycology 2005;43(Supplement_1):S197–202.
15. Stevens DA, Moss RB, Kurup VP, et al. Allergic Bronchopulmonary Aspergillosis in Cystic Fibrosis—State of the Art: Cystic Fibrosis Foundation Consensus Conference. Clinical Infectious Diseases 2003;37(Supplement_3):S225–64.
16. Asano K, Hebisawa A, Ishiguro T, et al. New clinical diagnostic criteria for allergic bronchopulmonary aspergillosis/mycosis and its validation. Journal of Allergy and Clinical Immunology 2021;147(4):1261-1268.e5.
17. Agarwal R. Severe asthma with fungal sensitization. Curr Allergy Asthma Rep 2011;11(5):403–13.
18. Schweer KE, Bangard C, Hekmat K, Cornely OA. Chronic pulmonary aspergillosis. Mycoses 2014;57(5):257–70.
19. Romani L. Immunity to fungal infections. Nat Rev Immunol 2004;4(1):11–24.
20. Denning DW, Riniotis K, Dobrashian R, Sambatakou H. Chronic Cavitary and Fibrosing Pulmonary and Pleural Aspergillosis: Case Series, Proposed Nomenclature Change, and Review. Clinical Infectious Diseases 2003;37(Supplement_3):S265–80.
21. Pagano L, Akova M, Dimopoulos G, Herbrecht R, Drgona L, Blijlevens N. Risk assessment and prognostic factors for mould-related diseases in immunocompromised patients. J Antimicrob Chemother 2011;66 Suppl 1:i5-14.
22. Lamoth F, Calandra T. Early diagnosis of invasive mould infections and disease. J Antimicrob Chemother 2017;72(suppl_1):i19–28.
23. Verweij PE, Rijnders BJA, Brüggemann RJM, et al. Review of influenza-associated pulmonary aspergillosis in ICU patients and proposal for a case definition: an expert opinion. Intensive Care Med 2020;46(8):1524–35.
24. Schauwvlieghe AFAD, Rijnders BJA, Philips N, et al. Invasive aspergillosis in patients admitted to the intensive care unit with severe influenza: a retrospective cohort study. The Lancet Respiratory Medicine 2018;6(10):782–92.
25. Koehler P, Cornely OA, Böttiger BW, et al. COVID-19 associated pulmonary aspergillosis. Mycoses 2020;63(6):528–34.
26. Donnelly JP, Chen SC, Kauffman CA, et al. Revision and Update of the Consensus Definitions of Invasive Fungal Disease From the European Organization for Research and Treatment of Cancer and the Mycoses Study Group Education and Research Consortium. Clin Infect Dis 2019;
27. Greene RE, Schlamm HT, Oestmann J-W, et al. Imaging Findings in Acute Invasive Pulmonary Aspergillosis: Clinical Significance of the Halo Sign. Clin Infect Dis 2007;44(3):373–9.
28. Alexander BD, Lamoth F, Heussel CP, et al. Guidance on Imaging for Invasive Pulmonary Aspergillosis and Mucormycosis: From the Imaging Working Group for the Revision and Update of the Consensus Definitions of Fungal Disease from the EORTC/MSGERC. Clinical Infectious Diseases 2021;72(Supplement_2):S79–88.
29. Henzler C, Henzler T, Buchheidt D, et al. Diagnostic Performance of Contrast Enhanced Pulmonary Computed Tomography Angiography for the Detection of Angioinvasive Pulmonary Aspergillosis in Immunocompromised Patients. Sci Rep 2017;7(1):4483.
30. Stanzani M, Battista G, Sassi C, et al. Computed Tomographic Pulmonary Angiography for Diagnosis of Invasive Mold Diseases in Patients With Hematological Malignancies. Clin Infect Dis 2012;54(5):610–6.
31. Miceli MH, Maertens J, Buvé K, et al. Immune reconstitution inflammatory syndrome in cancer patients with pulmonary aspergillosis recovering from neutropenia: Proof of principle, description, and clinical and research implications. Cancer 2007;110(1):112–20.
32. Segal BH, Herbrecht R, Stevens DA, et al. Defining Responses to Therapy and Study Outcomes in Clinical Trials of Invasive Fungal Diseases: Mycoses Study Group and European Organization for Research and Treatment of Cancer Consensus Criteria. Clin Infect Dis 2008;47(5):674–83.
33. Yagi A, Sato N, Takahashi A, et al. Added value of contrast-enhanced CISS imaging in relation to conventional MR images for the evaluation of intracavernous cranial nerve lesions. Neuroradiology 2010;52(12):1101–9.
34. Marzolf G, Sabou M, Lannes B, et al. Magnetic Resonance Imaging of Cerebral Aspergillosis: Imaging and Pathological Correlations. PLOS ONE 2016;11(4):e0152475.
35. Starkey J, Moritani T, Kirby P. MRI of CNS Fungal Infections: Review of Aspergillosis to Histoplasmosis and Everything in Between. Clin Neuroradiol 2014;24(3):217–30.
36. Sharma P, Mukherjee A, Karunanithi S, Bal C, Kumar R. Potential Role of 18F-FDG PET/CT in Patients With Fungal Infections. American Journal of Roentgenology 2014;203(1):180–9.
37. Cummings JR, Jamison GR, Boudreaux JW, Howles MJ, Walsh TJ, Hayden RT. Cross-reactivity of non-Aspergillus fungal species in the Aspergillus galactomannan enzyme immunoassay. Diagn Microbiol Infect Dis 2007;59(1):113–5.
38. Mikulska M, Furfaro E, Del Bono V, et al. Galactomannan testing might be useful for early diagnosis of fusariosis. Diagn Microbiol Infect Dis 2012;72(4):367–9.
39. Xavier MO, Pasqualotto AC, Cardoso ICE, Severo LC. Cross-Reactivity of Paracoccidioides brasiliensis, Histoplasma capsulatum, and Cryptococcus Species in the Commercial Platelia Aspergillus Enzyme Immunoassay. Clin Vaccine Immunol 2009;16(1):132–3.
40. Li X, Zheng Y, Wu F, et al. Evaluation of quantitative real-time PCR and Platelia galactomannan assays for the diagnosis of disseminated Talaromyces marneffei infection. Med Mycol 2020;58(2):181–6.
41. Mercier T, Castagnola E, Marr KA, Wheat LJ, Verweij PE, Maertens JA. Defining Galactomannan Positivity in the Updated EORTC/MSGERC Consensus Definitions of Invasive Fungal Diseases. Clin Infect Dis 2021;72(Suppl 2):S89–94.
42. Leeflang MMG, Debets-Ossenkopp YJ, Wang J, et al. Galactomannan detection for invasive aspergillosis in immunocompromised patients. Cochrane Database Syst Rev 2015;(12):CD007394.
43. Arvanitis M, Anagnostou T, Mylonakis E. Galactomannan and Polymerase Chain Reaction–Based Screening for Invasive Aspergillosis Among High-Risk Hematology Patients: A Diagnostic Meta-analysis. Clin Infect Dis 2015;61(8):1263–72.
44. Hage CA, Reynolds JM, Durkin M, Wheat LJ, Knox KS. Plasmalyte as a Cause of False-Positive Results for Aspergillus Galactomannan in Bronchoalveolar Lavage Fluid. J Clin Microbiol 2007;45(2):676–7.
45. Spriet I, Lagrou K, Maertens J, Willems L, Wilmer A, Wauters J. Plasmalyte: No Longer a Culprit in Causing False-Positive Galactomannan Test Results. Journal of Clinical Microbiology 2016;54(3):795–7.
46. Mercier T, Schauwvlieghe A, de Kort E, et al. Diagnosing invasive pulmonary aspergillosis in hematology patients: a retrospective multicenter evaluation of a novel lateral flow device. Journal of Clinical Microbiology 2019;JCM.01913-18.
47. Mercier T, Dunbar A, de Kort E, et al. Lateral flow assays for diagnosing invasive pulmonary aspergillosis in adult hematology patients: A comparative multicenter study. Med Mycol 2019;
48. Mercier T, Guldentops E, Lagrou K, Maertens J. Prospective evaluation of the turbidimetric β-D-glucan assay and two lateral flow assays on serum in invasive aspergillosis. Clin Infect Dis 2020;
49. He S, Hang J-P, Zhang L, Wang F, Zhang D-C, Gong F-H. A systematic review and meta-analysis of diagnostic accuracy of serum 1,3-β-D-glucan for invasive fungal infection: Focus on cutoff levels. J Microbiol Immunol Infect 2015;48(4):351–61.
50. Karageorgopoulos DE, Vouloumanou EK, Ntziora F, Michalopoulos A, Rafailidis PI, Falagas ME. β-D-Glucan Assay for the Diagnosis of Invasive Fungal Infections: A Meta-analysis. Clin Infect Dis 2011;52(6):750–70.
51. Karageorgopoulos DE, Qu J-M, Korbila IP, Zhu Y-G, Vasileiou VA, Falagas ME. Accuracy of β-D-glucan for the diagnosis of Pneumocystis jirovecii pneumonia: a meta-analysis. Clin Microbiol Infect 2013;19(1):39–49.
52. Li W-J, Guo Y-L, Liu T-J, Wang K, Kong J-L. Diagnosis of pneumocystis pneumonia using serum (1-3)-β-D-Glucan: a bivariate meta-analysis and systematic review. J Thorac Dis 2015;7(12):2214–25.
53. Onishi A, Sugiyama D, Kogata Y, et al. Diagnostic Accuracy of Serum 1,3-β-D-Glucan for Pneumocystis Jiroveci Pneumonia, Invasive Candidiasis and Invasive Aspergillosis: Systematic Review and Meta-Analysis. J Clin Microbiol 2011;JCM.05267-11.
54. Mercier T, Guldentops E, Patteet S, Beuselinck K, Lagrou K, Maertens J. Beta-d-Glucan for Diagnosing Pneumocystis Pneumonia: a Direct Comparison between the Wako β-Glucan Assay and the Fungitell Assay. J Clin Microbiol 2019;57(6).
55. Friedrich R, Rappold E, Bogdan C, Held J. Comparative Analysis of the Wako β-Glucan Test and the Fungitell Assay for Diagnosis of Candidemia and Pneumocystis jirovecii Pneumonia. J Clin Microbiol 2018;56(9).
56. Theel ES, Doern CD. β-d-Glucan Testing Is Important for Diagnosis of Invasive Fungal Infections. J Clin Microbiol 2013;51(11):3478–83.
57. Buil JB, Zoll J, Verweij PE, Melchers WJG. Molecular Detection of Azole-Resistant Aspergillus fumigatus in Clinical Samples. Front Microbiol 2018;9:515.
58. Hayette M-P, Vaira D, Susin F, et al. Detection of Aspergillus Species DNA by PCR in Bronchoalveolar Lavage Fluid. J Clin Microbiol 2001;39(6):2338–40.
59. Imbert S, Brossas J-Y, Palous M, Joly I, Meyer I, Fekkar A. Performance of Aspergillus PCR in cerebrospinal fluid for the diagnosis of cerebral aspergillosis. Clin Microbiol Infect 2017;23(11):889.e1-889.e4.
60. Reinwald M, Spiess B, Heinz WJ, et al. Aspergillus PCR-Based Investigation of Fresh Tissue and Effusion Samples in Patients with Suspected Invasive Aspergillosis Enhances Diagnostic Capabilities. J Clin Microbiol 2013;51(12):4178–85.
61. Cruciani M, Mengoli C, Barnes R, et al. Polymerase chain reaction blood tests for the diagnosis of invasive aspergillosis in immunocompromised people. Cochrane Database Syst Rev 2019;9(9):CD009551.
62. Verweij PE, Snelders E, Kema GH, Mellado E, Melchers WJ. Azole resistance in Aspergillus fumigatus: a side-effect of environmental fungicide use? The Lancet Infectious Diseases 2009;9(12):789–95.
63. Resendiz Sharpe A, Lagrou K, Meis JF, et al. Triazole resistance surveillance in Aspergillus fumigatus. Med Mycol 2018;56(suppl_1):83–92.
64. Mercier T, Reynders M, Beuselinck K, Guldentops E, Maertens J, Lagrou K. Serial Detection of Circulating Mucorales DNA in Invasive Mucormycosis: A Retrospective Multicenter Evaluation. J Fungi (Basel) 2019;5(4).
65. Millon L, Scherer E, Rocchi S, Bellanger A-P. Molecular Strategies to Diagnose Mucormycosis. Journal of Fungi 2019;5(1):24.
66. Arendrup MC, Bille J, Dannaoui E, Ruhnke M, Heussel C-P, Kibbler C. ECIL-3 classical diagnostic procedures for the diagnosis of invasive fungal diseases in patients with leukaemia. Bone Marrow Transplant 2012;47(8):1030–45.
67. Lestrade PPA, Buil JB, van der Beek MT, et al. Paradoxal Trends in Azole-Resistant Aspergillus fumigatus in a National Multicenter Surveillance Program, the Netherlands, 2013-2018. Emerg Infect Dis 2020;26(7):1447–55.
68. Arendrup MC, Verweij PE, Mouton JW, Lagrou K, Meletiadis J. Multicentre validation of 4-well azole agar plates as a screening method for detection of clinically relevant azole-resistant Aspergillus fumigatus. J Antimicrob Chemother 2017;72(12):3325–33.
69. Shah AA, Hazen KC. Diagnostic accuracy of histopathologic and cytopathologic examination of Aspergillus species. Am J Clin Pathol 2013;139(1):55–61.
70. Dutch SWAB Guidelines for the Management of Invasive Fungal Infections 2017
71. Lass-Flörl C, Samardzic E, Knoll M. Serology anno 2021-fungal infections: from invasive to chronic. Clin Microbiol Infect 2021;27(9):1230 -41.
72. Herbrecht R et al. Ann N Y Acad Sci. 2012; 1272: 23-30

Dit stuk bevat educatieve informatie over een ziektebeeld en/ of medische aandoening en is uitsluitend bedoeld voor beroepsbeoefenaren. Gilead beoogt geen behandeladvies te geven. Het bevat vertrouwelijke en beschermde informatie van Gilead en mag niet geheel of gedeeltelijk worden gekopieerd, gebruikt of verspreid voor welk doel dan ook, behalve voor uw eigen educatief gebruik, zonder de voorafgaande schriftelijke toestemming van Gilead.
Copyright 2023 Gilead Sciences Netherlands B.V. All rights reserverd. Website privacy statement. Terms of use GILEAD and the GILEAD Logo are trademarks of Gilead Sciences, inc.
NL-AMB-0209
